- Partikel Penyusun Atom
Teori atom Dalton menyatakan bahwa atom merupakan bagian terkecil dari materi. Pada kenyataannya, atom dapat dibagi menjadi partikel penyusunnya yaitu elektron, neutron dan proton. Hal ini dibuktikan berdasarkan penelitian tentang arus listrik pada gas bertekanan rendah. Penelitian dimulai pada tahun 1855 oleh Heinrich Geissler, yang berhasil merancang tabung gelas bertekanan rendah yang disebut tabung Geissler. Pada tahun 1859, Julius Plucker menggunakan tabung Geissler alam percobaan elektrolisis gas, didalam tabung ia memasang 2 plat elektrode, elektrode pada kutub positif disebut anode, sedangkan elektrode pada kutub positif disebut katode. Setelah diberi tegangan tinggi, ia mengamati adanya berkas sinar yang dipancarkan dari katode. Namun Plucker menganggap sinar tersebut sebagai cahaya listrik biasa.
Pada tahun 1876, Eugene Goldstein, menggunakan teknik yang sama dengan Plucker, namun ia menamakan berkas sinar yang dipancarkan dari katode sebagai sinar katode. Pertanyaan yang muncul adalah apakah sinar katode itu sebagai gelombang elektromagnetik atau partikel?
Wiliam Crookes, pada tahun 1880, memodifikasi tabung Geissler untuk membuat vakum lebih baik, tabung ini disebut sebagi tabung Crookes. Pengamatan Crookes tehadap karakteristik sinar katode dapat disimpulkan sebagai berikut:
Sinar katode merambat lurus.
Sinar katode membawa muatan karena dibelokkan dalam medan magnet.
Sinar katode memiliki massa karena dapat memutar kincir kecil dalam tabung.
Sinar katode menyebabkan materi seperti gas dan zat lain berpijar.
Akhirnya Crookes menyimpulkan bahwa sinar katode adalah partikel bermuatan.
Pada tahun 1891, George Johnston Stoney, berpendapat bahwa sinar katode adalah partikel, ia menamakan sebagai elektron. Pada tahun 1897, J.J. Thomson membuktikan bahwa sinar katode adalah merupakan berkas partikel, dengan menggunakan tabung sinar katode khusus.
Proton,
Pada tahun 1886, Eugene Goldstein, membuktikan adanya muatan positif. Pembuktian dilakukan menggunakan tabung sinar katode dimana plat katode telah diberi lubang. Ia mengamati jalannya sinar katode yang merambat menuju anode, tenyata terdapat sinar lain yang bergerak dengan arah berlawanan melewati lubang pada plat katode. Oleh karena arahnya berlawanan, maka sinar tersebut haruslah terdiri dari muatan positif.
Neutron.
Penemuan partikel neutron diawali oleh penelitian Rutherford, dalam eksperimennya ia berusaha menghitung jumlah muatan positif dalam inti atom dan massa inti atom dan ia mendapati bahwa massa inti atom hanya setengah dari massa atom. Pada tahun 1920, William Draper Harkins, berasumsi bahwa terdapat partikel lain dalam inti atom selain proton, partikel itu bermassa hampir sama dengan proton dan tidak bermuatan, ia menyebutnya sebagai neutron. Hingga tahun 1932, James Chadwick, membuktikan keberadaan partikel neutron.
Adanya penemuan neutron ini, membuat strukur atom semakin jelas, bahwa atom tersusun atas inti atom dengan elektron mengelilingi pada lintasan kulitnya. Inti atom terdiri dari proton yang bermuatan positif dan neutron yang tidak bermuatan. Sedangkan elektron bermuatan negatif.
Sumber: http://liakimiapasca.wordpress.com/kimia-kelas-x/struktur-atom/b-partikel-dasar-penyusun-atom/
- Nomor Atom dan Nomor Massa


- Isotop, Isoton, Isobar

Setiap karbon mempunyai nomor atom 6 tetapi nomor massanya berbeda-beda. Dari contoh tersebut dapat dikatakan bahwa walaupun unsurnya sama belum tentu nomor massanya sama.
Isobar dan Isoton
Isobar adalah atom unsur yang berbeda tetapi mempunyai nomor massa sama. Isobar dapat dimengerti dengan melihat contoh berupa  dengan
dengan  yang memiliki nomor massa sebesar 24. Sedangkan isoton adalaha tom unsur yang berbeda tetapi mempunyai jumlah netron yang sama. Contoh isoton adalah
yang memiliki nomor massa sebesar 24. Sedangkan isoton adalaha tom unsur yang berbeda tetapi mempunyai jumlah netron yang sama. Contoh isoton adalah  yang sama-sama memiliki jumlah neutron 20.
yang sama-sama memiliki jumlah neutron 20.
Perbedaan isotop, isoton dan isobar yaituisotop adalah atom unsur sama dengan nomor massa berbeda. Isotop dapat juga dikatakan sebagai atom unsur yang mempunyai nomor atom sama tetapi mempunyai nomor massa berbeda karena setiap unsur mempunyai nomor atom yang berbedaisoton adalah atom unsur yang berbeda tetapi mempunyai nomor massa sama. Contoh isoton adalah rm10 yang sama-sama memiliki jumlah neutron 20.
Isobar dapat dimengerti dengan melihat contoh berupa rm111 dengan rm9 yang memiliki nomor massa sebesar 24tom unsur yang berbeda tetapi mempunyai jumlah netron yang sama.
- Massa Atom Relatif: Standar Massa Atom, Ar dan Mr
Massa atom relatif (Ar) merupakan perbandingan massa atom dengan massa satu atom yang tetap. Standar massa atom yang digunakan adalah massa atom 12C.
Dalam tabel periodik, (Ar) diletakkan dibawah lambang unsurnya.
Massa Molekul Relatif (Mr)
Massa molekul relatif (Mr) merupakan penjumlahan dari massa atom relatif. Jadi, massa molekul relatif dapat dirumuskan sebagai berikut.
- Struktur / Teori Atom: Model Atom Dalton, Model Atom Thompson, Model Atom Rutherford, Model Atom Bohr
Macam Macam Model Atom : John Dalton, J.J. Thomson, Rutherford, Niels Bohr
Dalton mengatakan bahwa atom atom seperti bola pejal atau bola tolak peluru JJ.Thomson mengatakan bahwa atomm seperti roti kismis E.Rutherford mengemukakan atom seperti tata surya
Kelemahan model Thomson ini tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola atom tersebut.
Kelemahan model atom Thomson
Model Thomson ini tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola atom tersebut.
Rutherford melakukan penelitian tentang hamburan sinar α pada lempeng emas. Hasil pengamatan tersebut dikembangkan dalam hipotesis model atom Rutherford.
a. Sebagian besar dari atom merupakan permukaan kosong.
b. Atom memiliki inti atom bermuatan positif yang merupakan pusat massa atom.
c. Elektron bergerak mengelilingi inti dengan kecepatan yang sangat tinggi.
d. Sebagian besar partikel α lewat tanpa mengalami pembelokkan/hambatan. Sebagian kecil dibelokkan, dan sedikit sekali yang dipantulkan.
Kelemahan Model Atom Rutherford
a. Menurut hukum fisika klasik, elektron yang bergerak mengelilingi inti memancarkan energi dalam bentuk gelombang elektromagnetik. Akibatnya, lama-kelamaan elektron itu akan kehabisan energi dan akhirnya menempel pada inti.
b. Model atom rutherford ini belum mampu menjelaskan dimana letak elektron dan cara rotasinya terhadap inti atom.
c. Elektron memancarkan energi ketika bergerak, sehingga energi atom menjadi tidak stabil.
d. Tidak dapat menjelaskan spektrum garis pada atom hidrogen (H).
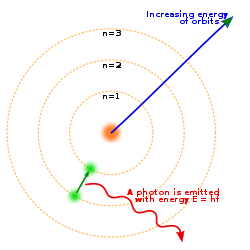
Pada tahun 1913, Niels Bohr mengemukakan pendapatnya bahwa elektron bergerak mengelilingi inti atom pada lintasan-lintasan tertentu yang disebut kulit atom. Model atom Bohr merupakan penyempurnaan dari model atom Rutherford.
Kelemahan teori atom Rutherford diperbaiki oleh Neils Bohr dengan postulat bohr :
a. Elektron-elektron yang mengelilingi inti mempunyai lintasan dan energi tertentu.
b. Dalam orbital tertentu, energi elektron adalah tetap. Elektron akan menyerap energi jika berpindah ke orbit yang lebih luar dan akan membebaskan energi jika berpindah ke orbit yang lebih dalam
Kelebihan model atom Bohr
atom terdiri dari beberapa kulit untuk tempat berpindahnya elektron.
Kelemahan model atom Bohr
a. tidak dapat menjelaskan efek Zeeman dan efek Strack.
b. Tidak dapat menerangkan kejadian-kejadian dalam ikatan kimia dengan baik, pengaruh medan magnet terhadap atom-atom, dan spektrum atom yang berelektron lebih banyak.
sumber
Dalton mengatakan bahwa atom atom seperti bola pejal atau bola tolak peluru JJ.Thomson mengatakan bahwa atomm seperti roti kismis E.Rutherford mengemukakan atom seperti tata surya
1. Model Atom John Dalton
Pada tahun 1808, John Dalton yang merupakan seorang guru di Inggris, melakukan perenungan tentang atom. Hasil perenungan Dalton menyempurnakan teori atom Democritus. Bayangan Dalton dan Democritus adalah bahwa atom berbentuk pejal.. Dalam renungannya Dalton mengemukakan postulatnya tentang atom:- Setiap unsur terdiri dari partikel yang sangat kecil yang dinamakan dengan atom
- Atom dari unsur yang sama memiliiki sifat yang sama
- Atom dari unsur berbeda memiliki sifat yang berbeda pula
- Atom dari suatu unsur tidak dapat diubah menjadi atom unsur lain dengan reaksi kimia, atom tidak dapat dimusnahkan dan atom juga tidak dapat dihancurkan
- Atom-atom dapat bergabung membentuk gabungan atom yang disebut molekul
- Dalam senyawa, perbandingan massa masing-masing unsur adalah tetap
2. Model Atom J.J. Thomson
Kelemahan dari Dalton diperbaiki oleh JJ. Thomson, eksperimen yang dilakukannya tabung sinar kotoda. Hasil eksperimennya menyatakan ada partikel bermuatan negatif dalam atom yang disebut elektron. Suatu bola pejal yang permukaannya dikelilingi elektron dan partikel lain yang bermuatan positif sehingga atom bersifat netral. Gambar atom model Thomson :Kelemahan model Thomson ini tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola atom tersebut.
Kelemahan model atom Thomson
Model Thomson ini tidak dapat menjelaskan susunan muatan positif dan negatif dalam bola atom tersebut.
3. Model Atom Rutherford
Model atom Rutherford
a. Sebagian besar dari atom merupakan permukaan kosong.
b. Atom memiliki inti atom bermuatan positif yang merupakan pusat massa atom.
c. Elektron bergerak mengelilingi inti dengan kecepatan yang sangat tinggi.
d. Sebagian besar partikel α lewat tanpa mengalami pembelokkan/hambatan. Sebagian kecil dibelokkan, dan sedikit sekali yang dipantulkan.
Kelemahan Model Atom Rutherford
a. Menurut hukum fisika klasik, elektron yang bergerak mengelilingi inti memancarkan energi dalam bentuk gelombang elektromagnetik. Akibatnya, lama-kelamaan elektron itu akan kehabisan energi dan akhirnya menempel pada inti.
b. Model atom rutherford ini belum mampu menjelaskan dimana letak elektron dan cara rotasinya terhadap inti atom.
c. Elektron memancarkan energi ketika bergerak, sehingga energi atom menjadi tidak stabil.
d. Tidak dapat menjelaskan spektrum garis pada atom hidrogen (H).
4. Model Atom Niels Bohr
Model Atom Niels Bohr
Pada tahun 1913, Niels Bohr mengemukakan pendapatnya bahwa elektron bergerak mengelilingi inti atom pada lintasan-lintasan tertentu yang disebut kulit atom. Model atom Bohr merupakan penyempurnaan dari model atom Rutherford.
Kelemahan teori atom Rutherford diperbaiki oleh Neils Bohr dengan postulat bohr :
a. Elektron-elektron yang mengelilingi inti mempunyai lintasan dan energi tertentu.
b. Dalam orbital tertentu, energi elektron adalah tetap. Elektron akan menyerap energi jika berpindah ke orbit yang lebih luar dan akan membebaskan energi jika berpindah ke orbit yang lebih dalam
Kelebihan model atom Bohr
atom terdiri dari beberapa kulit untuk tempat berpindahnya elektron.
Kelemahan model atom Bohr
a. tidak dapat menjelaskan efek Zeeman dan efek Strack.
b. Tidak dapat menerangkan kejadian-kejadian dalam ikatan kimia dengan baik, pengaruh medan magnet terhadap atom-atom, dan spektrum atom yang berelektron lebih banyak.
sumber
- Konfigurasi Elektron dan Elektron Valensi
Ialah susunan elektron suatu atom berdasarkan kulit-kulit atom tersebut.
Setiap kulit atom dapat terisi elektron maksimum dengan rumus:

Gambar.12. Jumlah elektron maksimum tiap kulit dalam atom
Keterangan :
- ∑ = jumlah maksimum elektron pada suatu kulit
- n = nomor kulit

Keterangan gambar: Jumlah elektron maksimum tiap kulit dalam atom
Jumlah elektron maksimum dalam tiap-tiap kulit atom

Aturan-aturan dalam pengisian konfigurasi elektron:
1.Pengisian dimulai dari tingkat energi paling rendah ketingkat energi paling tinggi dari kulit K, L,M dan seterusnya
2.Jika jumlah elektron yang tersisa ≤ 8 di tempatkan pada kulit berikutnya
3.Jumlah maksimum elektron pada kulit terluar adalah 8
Contoh soal :
Tulislah konfigurasi elektron dari:

Jawab.
1. Jumlah elektron = 8
Konfigurasi elektron K= 2 L= 6
2.Jumlah elektron = 18
Konfigurasi elektron K= 2 L= 8 M= 8
3.Jumlah elektron = 38
Konfigurasi elektron K= 2 L=8 M= 18 N=8 O=2
2. Elektron Valensi
Elektron valensi ialah jumlah elektron pada kulit terluar suatu atom netral. Cara
menentukan elektron valensi adalah dengan menuliskan konfigurasi elektron.
Contoh soal:
Tulislah konfigurasi elektron dan elektron valensi dari atom-atom berikut:

Jawab:
1. Nomor atom = 20, jumlah elektron=20
Konfigurasi elektron K=2 L=8 M=8 N=2
Elektron valensi =2
2. Nomor atom = 35
Konfigurasi elektron K=2 L=8 M=18 N=7
Elektron valensi =7
 20.50
20.50
 Unknown
Unknown





0 komentar :
Posting Komentar